質量数と同位体 [理科]
原子は、その中心に大きさに比べはるかに小さい、陽子と中性子からなる原子核と
そのまわりの決まった軌道上に電子(e ̄)があり、
その軌道の大きさで、原子の大きさは、決定され、
プラスの電気を持つ陽子の数とマイナスの電気を持つ電子(e ̄)が同数のとき、
原子は、電気的に釣合っており、
イオンは、電子(e ̄)の数が違うため、電気を帯びています。
今度は原子の重さについて考えてみましょう。
電子は考慮に入れ無くていいくらいの、重さしかないので、
原子核にある、陽子の個数と中性子の個数を足した
質量数で、表現します。
元素記号の左上に質量数は書きます。
例えば
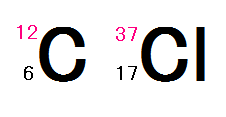
左は原子番号6の炭素質量数12を表し、中性子の数は6
右は原子番号17の塩素質量数37を表し、中性子の数は20になります。
そして同位体とは、同じ元素でも質量数が違う
( つまり中性子の数が違う )原子を言います。
自然界にある、元素は複数の同位体が固有の割合で混在しているものも多くあります。
例えば炭素には、質量数13のものが少量、塩素では、質量数35のものが大半です。
質量数が違っても、同じ元素であれば、化学的性質の違いは、極めて僅かです。
原子の外側の電子が、それをほとんど決めるからです。
神様は、電子軌道の空間を、大きくし過ぎたようで、
生物からモノ全てどんなに重くてもスカスカとも考えられます。
でも、2桁くらいの原子番号から偶数の元素は、同位体の数が多く
奇数の元素は、同位体の数が少ないようにしているようです。
これは原子核の陽子の個数が、偶数のときは、中性子の個数は、偶数も奇数もあるのに、
陽子の個数が、奇数になると、中性子の個数は偶数だけになる傾向があるからようです。
んー何かありそうな。もったえぶりです。
なお、同位体の数が多いから、その元素が多くあるとは限りません。
多品種少量タイプもイメージしてみてください。
また、半減期のある程度ある同位体・人工同位体は、考慮していません。
そのまわりの決まった軌道上に電子(e ̄)があり、
その軌道の大きさで、原子の大きさは、決定され、
プラスの電気を持つ陽子の数とマイナスの電気を持つ電子(e ̄)が同数のとき、
原子は、電気的に釣合っており、
イオンは、電子(e ̄)の数が違うため、電気を帯びています。
今度は原子の重さについて考えてみましょう。
電子は考慮に入れ無くていいくらいの、重さしかないので、
原子核にある、陽子の個数と中性子の個数を足した
質量数で、表現します。
元素記号の左上に質量数は書きます。
例えば
左は原子番号6の炭素質量数12を表し、中性子の数は6
右は原子番号17の塩素質量数37を表し、中性子の数は20になります。
そして同位体とは、同じ元素でも質量数が違う
( つまり中性子の数が違う )原子を言います。
自然界にある、元素は複数の同位体が固有の割合で混在しているものも多くあります。
例えば炭素には、質量数13のものが少量、塩素では、質量数35のものが大半です。
質量数が違っても、同じ元素であれば、化学的性質の違いは、極めて僅かです。
原子の外側の電子が、それをほとんど決めるからです。
神様は、電子軌道の空間を、大きくし過ぎたようで、
生物からモノ全てどんなに重くてもスカスカとも考えられます。
でも、2桁くらいの原子番号から偶数の元素は、同位体の数が多く
奇数の元素は、同位体の数が少ないようにしているようです。
これは原子核の陽子の個数が、偶数のときは、中性子の個数は、偶数も奇数もあるのに、
陽子の個数が、奇数になると、中性子の個数は偶数だけになる傾向があるからようです。
んー何かありそうな。もったえぶりです。
なお、同位体の数が多いから、その元素が多くあるとは限りません。
多品種少量タイプもイメージしてみてください。
また、半減期のある程度ある同位体・人工同位体は、考慮していません。




コメント 0